뉴스룸저널클럽
- Adjunctive Intravenous Argatroban or Eptifibatide for Ischemic Stroke
-
- 관리자
- 2024-11-01
- 조회수 : 892
Link URL : https://
Adjunctive Intravenous Argatroban or Eptifibatide for Ischemic Stroke
Adeoye O., et al. N Engl J Med 2024;391:810-20.
MOST (Multi-arm Optimization of Stroke Thrombolysis) 임상연구는 급성 허혈뇌졸중 환자에서 정맥 내 혈전용해술(IV thrombolysis) 단독 치료와 Argatroban (항응고제), Eptifibatide (항혈소판제) 보조 치료의 효능과 안전성을 평가하기 위해 수행된 다기관, 무작위, 단일 맹검 3상 임상 시험이다. 증상 발생 3시간 이내 정맥내 혈전용해 치료를 받은 후 75분 이내에 무작위 배정, 추가적인 보조 치료 시작이 가능한 급성 허혈뇌졸중 환자를 대상으로 하였다.
연구 목적은 정맥내 혈전용해술 후 Argatroban 또는 Eptifibatide가 급성 허혈뇌졸중 환자에서 90일 후 장애를 줄이는 데 효과를 알아보는 것으로 주요 유효성 평가는 90일 뒤 mRS 점수를 유틸리티 가중치로 평가하였고, 주요 안전성 평가는 36시간 내 증상두개내출혈(symptomatic intracranial hemorrhage, sICH)의 발생률이었다.
- MOST 다단계 무작위 배정
-
- 초기 고정 배정(1:1:1): 첫 150명은 각 군에 1:1:1 비율로 고정된 무작위 배정
- 반응 적응 무작위 배정(Response-Adaptive Randomization, RAR): 150번째 환자부터 무작위 배정 확률을 조정. 초기 데이터 기반의 치료 효과를 예측 후 효과가 큰 것으로 보이는 치료군에 환자가 더 많이 배정.
- 후반 고정 배정: 500명 이후 등록 이후 각 치료군 간 비교의 일관성을 높이기 위해 고정된 비율로 무작위 배정 방식을 계획.
그러나, MOST 임상 시험은 2018년에 시작되어 2023년 중간 분석 후 종료되었다. 미국의 57개 병원에서 환자를 모집했으며, 초기 등록 목표는 1200명이었으나, 500명 등록 후 중간 분석에서 두 보조 치료(Argatroban 및 Eptifibatide)가 유의미한 치료 효과를 보이지 않는다는 결과가 나오면서 연구가 조기 종료되었다.
총 514명의 환자가 세 그룹으로 무작위 배정되어, Argatroban 그룹(59명), Eptifibatide 그룹(227명), 그리고 위약 그룹(228명)으로 구성되었으며, 모든 환자는 정맥 내 혈전용해술을 받았다(70%는 Alteplase, 30%는 Tenecteplase). 이 중 약 44%가 혈관내혈전제거술을 받았다.
주요 연구 결과로 90일 후 유틸리티 가중 mRS 점수는 Argatroban 그룹에서 평균 5.2, Eptifibatide 그룹에서 6.3, 위약 그룹에서 6.8로 Argatroban과 위약 비교의 후향적 우월 확률은 0.002였으며, Eptifibatide와 위약의 비교 확률은 0.041로 두 보조 치료 모두 유의미한 효과를 보이지 않았다. sICH 발생률은 Argatroban 4%, Eptifibatide 3%, 위약 2%로 세 그룹 간 유사하였다. 90일 사망률은 Argatroban 24%, Eptifibatide 12%, 위약 8%로 Argatroban 그룹에서 높게 나타났다.
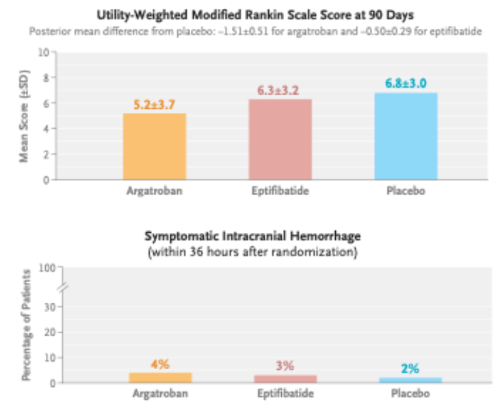
MOST 시험은 급성 허혈뇌졸중 환자에서 추가적인 Argatroban 또는 Eptifibatide의 보조 치료가 90일 후 장애를 줄이지 못했으며, 특히 Argatroban 그룹에서 사망률이 증가하였다. 이는 두 약물이 표준 혈전치료에 보조치료로 사용될 경우 안정성 문제가 있으며, 혈전용해치료에 대한 보조치료가 필요한 것을 아니라는 점을 시사한다.

 HOME
HOME LOGIN
LOGIN
